Nomeclatura de Compostos Organicos e Inorgânicos -ENEM 2013
Questão Exemplo
No ano de 2004, diversas mortes de animais por envenenamento no zoológico de São Paulo foram evidenciadas. Estudos técnicos apontam suspeita de intoxicação por monofluoracetato de sódio, conhecido como composto 1080 e ilegalmente comercializado como raticida. O monofluoracetato de sódio é um derivado do ácido monofluoracético e age no organismo dos mamíferos bloqueando o ciclo de Krebs, que pode levar à parada da respiração celular oxidativa e ao acúmulo de amônia na circulação.

monofluoracetato de sódio
Disponível: http//www1.folha.uol.com.br. Acesso em: 5 ago. 2010 (adaptado).
O monofluoracetato de sódio pode ser obtido pela
Os sais orgânicos são compostos obtidos por meio da reação entre um ácido carboxílico e uma base inorgânica, em que o hidrogênio do grupo carboxila do ácido reage com o ânion hidróxido da base, formando água; enquanto o ânion orgânico une-se ao cátion da base para formar esse sal.
Isso significa que os sais orgânicos sempre possuem o grupo funcional:
.jpg)
A IUPAC estipulou algumas regras oficiais para a nomenclatura desses compostos, mostradas abaixo:

Veja os exemplos:
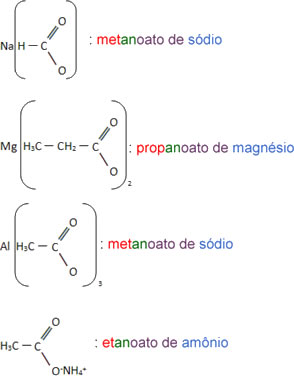
Se houver ramificações ou insaturações na cadeia carbônica será necessário numerá-la começando do carbono do grupo carboxila, como mostrado nos exemplos a seguir:
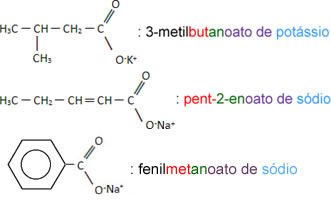
Além disso, quando um diácido carboxílico produzir sais orgânicos com substituição das duas extremidades da cadeia, basta colocar o prefixo di na nomenclatura, como no exemplo abaixo:

Um exemplo desse tipo de sal orgânico é o etanodiato de cálcio, que é um dos componentes mais comuns das pedras nos rins ou cálculos renais. O nome usual desse sal éoxalato de cálcio.
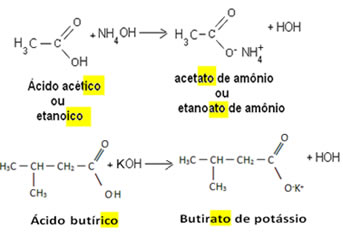
A nomenclatura usual dos sais orgânicos segue a mesma regra usada em Química Geral, sendo que quando um ácido inorgânico reage com uma base e dá origem a um sal, o nome do sal é feito partindo-se do nome do ácido de origem e mudando apenas a terminação.Quando termina com ico, mudamos para ato. Isso também é feito com os sais orgânicos, veja os exemplos:
Ácidos
São divididos em dois subgrupos:
- Hidrácidos (não apresentam átomos de oxigênio, formados por hidrogênio mais um elemento)
- Oxiácidos (apresentam átomos de oxigênio; formados por hidrogênio, oxigênio mais um elemento)
Nomenclatura dos Hidrácidos[editar]
- Ácido Nome do elemento químico ligado ao hidrogênio + ídrico
Exemplos:
- ácido clorídrico (HCl)
- ácido bromídrico (HBr)
- ácido fluorídrico (HF)
- ácido iodídrico (HI)
- ácido sulfídrico (H2S)
- ácido cianídrico (HCN)
Nomenclatura dos Oxiácidos[editar]
- Ácido + prefixo (se necessário) + elemento central + sufixo
De acordo com o elemento central (o primeiro é o hidrogênio e o terceiro é o oxigênio) temos o sufixo OSO para o menor NOx (Número de Oxidação) e ICO para o maior NOx:
- Coluna 14 ou 4A: - ácido carbônico (H2CO3) - carbono (C) com Número de Oxidação (NOx) = +4 (único ácido inorgânico com carbono).
- Coluna 15 ou 5A:
- ácido nitroso (HNO2) - nitrogênio (N) com NOx = +3;
- ácido nítrico (HNO3) - nitrogênio (N) com NOx = +5.
- Coluna 16 ou 6A:
- Coluna 17 ou 7A:
- ácido hipocloroso (HClO) - cloro (Cl) com NOx = +1 (o prefixo HIPO é obrigatório quando temos o elemento central com carga 1);
- ácido cloroso (HClO2) - cloro (Cl) com NOx = +3;
- ácido clórico (HClO3) - cloro (Cl) com NOx = +5;
- ácido perclórico (HClO4) - cloro (Cl) com NOx do Cl = +7 (o prefixo PER é obrigatório quando temos o elemento central com carga 7, como em Permanganato de potássio).
Observações:
- seguem a mesma nomenclatura os ácidos formados pelos elementos iodo (I) e bromo (Br), pertencentes também à coluna 17 ou 7A;
- o elemento flúor (F) também pertencente à coluna 17 ou 7A não forma oxiácidos.
Bases[editar]
Caracterizada por apresentar como único ânion o grupo hidroxila (OH)-.
Nomenclatura:
1ª maneira:
- Hidróxido de (Nome do metal ou grupo ligado á hidroxila) - usado quando o metal ou grupo ligado à hidroxila possui apenas um NOx.
Exemplos:
- hidróxido de sódio (NaOH);
- hidróxido de amônio (NH4OH);
- hidróxido de alumínio (Al(OH)3)
2ª maneira (quando o metal tem 2 NOx):
Hidróxido de (nome do metal) seguido do sufixo oso (para o menor NOx) ou ico (para o maior NOx)
Exemplos:
- hidróxido férrico {Fe(OH)3} - ferro (Fe) com NOx = +3;
- hidróxido ferroso {Fe(OH)2} - ferro (Fe) com NOx = +2.
3ª maneira (quando o metal tem 2 ou mais NOx):
Hidróxido de (nome do metal) + NOx em algarismos romanos (opcionalmente entre parêntesis)
- hidróxido de ferro (III) {Fe(OH)3} - ferro (Fe) com NOx = +3;
- hidróxido de ferro (II) {Fe(OH)2} - ferro (Fe) com NOx = +2.
Observação:
- Como a carga da Hidroxila, (OH)-, é sempre igual a -1, para identificar o NOx do metal ou grupo ligado à hidroxila, basta olhar qual o índice do grupo OH (na fórmula):
- KOH - como não há índice no grupo OH, indica que a carga do metal potássio é +1;
- Ca(OH)2 - o índice 2 indica que a carga do cálcio é +2;
- Al(OH)3 - o índice 3 indica que a carga do alumínio é +3;
- Pb(OH)4 - o índice 4 indica que a carga do chumbo (Pb) é +4.
Sais[editar]
Compostos inorgânicos com um pelo menos um Cátion diferente de H+ e pelo menos um ânion diferente de (OH)-.
Existem 3 subgrupos: Sais neutros, Sais ácidos e Sais básicos, tendo cada grupo uma diferença na nomenclatura pois, a nomenclatura depende dos reagentes envolvidos da reação de neutralização que forma o sal em questão.
Sais neutros[editar]
Uma reação comum de formação de sais é: ácido + base = sal + água.
Assim, o nome do sal deriva do ácido e da base que o formam. A primeira parte do nome do sal (ânion) deriva do ácido, com a seguinte variação:
Sufixo do sal | Sufixo do ácido
- eto | ídrico
- ito | oso
- ato | ico
Existem algumas mnemónicas para memorizá-la:
Mosquito teimoso te mato, te pico e te meto no vidríco
Perigoso mosquito no Bico do pato
Bico de Pato, Formoso Periquito, com ácido clorídrico não me meto
Bico de Pato, Osso de Cabrito, Frederico no espeto.
Exemplo[editar]
- HCl + NaOH = NaCl + H2O
- Ácido + Base = Sal + Água
- ácido clorídrico + hidróxido de sódio = cloreto de sódio + água
O ácido clorídrico doou o ânion Cl- que passou a chamar cloreto;
O hidróxido de sódio doou o cation Na+, que manteve o nome, sódio.
Sais Ácidos ou Hidrogenossais[editar]
São sais provenientes da neutralização parcial de um ácido, resultando num sal que possui pelo menos um átomo de hidrogênio que não foi neutralizado pela base.
- Sal = (Mono/Di/Tri/etc. Hidrogeno) + (Nome do ânion) + (Nome do Cátion)
Exemplo[editar]
- H3PO4 + NaOH = NaH2PO4 + H2O
- (Ácido) + (Base) = (Sal ácido) + água
- (Ácido fosfórico) + (Hidróxido de sódio) = (Diidrogeno fosfato de sódio) + água
NaH2PO4 - Diidrogeno fosfato de sódio (cuidado para não colocar o h do hidrogeno, pois não existe em português desta forma!!!);
Obs.: nomenclatura comum para sais ácidos:
NaHCO3 - hidrogeno carbonato de sódio (nome oficial), bicarbonato de sódio (nome comum), carbonato ácido de sódio (nome comum).
Sais básicos ou hidroxissais[editar]
São sais provenientes da neutralização parcial de uma base, resultando num sal que possui pelo menos uma hidroxila que não foi neutralizada pelo ácido.
(Mono/Di/Tri/etc. + hidróxi) + (nome do ânion) + (nome do cátion)
Exemplo[editar]
- HNO3 + Ca(OH)2 = Ca(OH)NO3 + H2O
- (Ácido) + (Base) = água + (Sal básico)
- (Ácido nítrico) + (Hidróxido de cálcio) = (hidróxi nitrato de cálcio + água)
Obs.: podemos também escrever monoidróxi nitrato de cálcio.
Pb(OH)3Cl - triidróxi cloreto de chumbo IV (ou plumbico);
Pb(OH)2Cl2 - diidróxi cloreto de chumbo IV (ou plumbico).
Obs.: nomes comuns para sais
Pb(OH)3Cl - cloreto tribásico de chumbo IV (ou plumbico);
Pb(OH)2Cl2 -cloreto dibásico de chumbo IV (ou plumbico).
Óxidos[editar]
São divididos em 4 subgrupos: Óxidos Básicos, Óxidos Ácidos, Óxidos Neutros, Óxidos Anfóteros e Óxidos Salinos(ou Duplos).
Óxidos básicos[editar]
São formados por metais das famílias 1A ou 2A + oxigênio esses óxidos reagem com a água para formar bases e reagem com ácidos para formar sal + água.
Óxido Básico + água = Na2O + H2O --> 2 NaOH
Óxido Básico + Ácido = Na2O + H2SO4 --> Na2SO4
- Óxido de (Nome do Metal) - o nome do metal poderá ser acompanhado pelos sufixos OSO/ICO ou NOx em algarismos romanos quando o metal tiver mais de um NOx.
Exemplos:
- Na2O - óxido de sódio
Óxidos ácidos (também chamados Anidridos)[editar]
São formados por oxigênio + ametal e reagem com a água para formar ácidos.
- (Mono/Di/Tri/Tetra/etc...) + óxido de + (Mono/Di/Tri/Tetra/etc...)(Nome do Ametal)
Em alguns casos, usa-se o nome anidrido, normalmente para ametais que formam vários óxidos.
- anidrido + [hipo ou per](Nome do Ametal)(ico ou oso)
Exemplos:
- CO2 - dióxido de carbono;
Óxidos neutros[editar]
Não reagem com a água, mas reagem com oxigênio quando for possível aumentar o NOX do cátion. Muitas vezes não existe uma regra geral para estes compostos.
Exemplo:
- CO - monóxido de carbono
- NO - óxido nítrico
- NO2 - dióxido de nitrogênio
Óxidos Anfóteros[editar]
Reagem com a água podendo formar ácidos ou bases.
Exemplo:
ZnO - óxido de zinco.
Óxidos salinos (ou duplos)[editar]
São formados da junção de dois óxidos, do mesmo metal, com nox diferentes. Reagem apenas com ácidos fortes. Com exceção do Pb2O3, os cátions possuem NOX +8/3.
- Óxido + duplo/salino de + nome do metal + nox dos óxidos formadores
Exemplo:
Hidretos Metálicos[editar]
São compostos inorgânicos nos quais temos um metal ligado ao hidrogênio, tendo o hidrogênio NOx = -1.
- Nomenclatura - (Hidreto de) + (nome do metal)
Exemplos:
- NaH - hidreto de sódio;
- LiH - hidreto de lítio;
- KH - hidreto de potássio;
- MgH2 - hidreto de magnésio.
Peróxidos[editar]
São compostos inorgânicos que possuem em sua estrutura (O2)-2 + metal. O NOx do oxigênio nestes compostos vale -1.
- Nomenclatura - (Peróxido de) + (nome do metal)
Exemplos:
- MgO2 - peróxido de magnésio.
Obs.: apesar das fórmulas possuírem índices iguais, não podemos simplificá-las como escrever HO ao invés de H2O2, pois a simplificação não mostra a realidade do composto!!!


Comentários